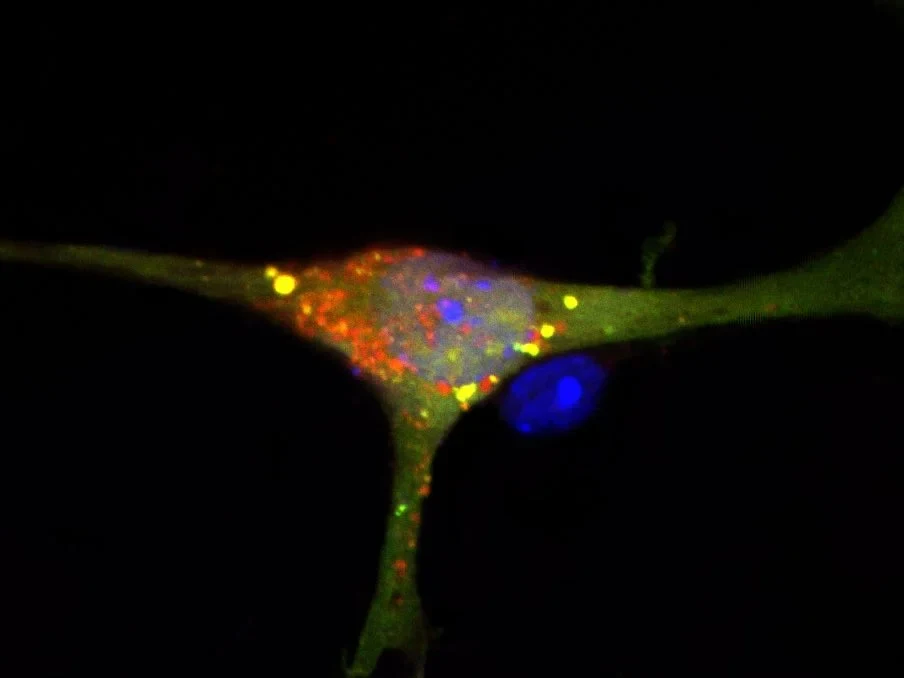
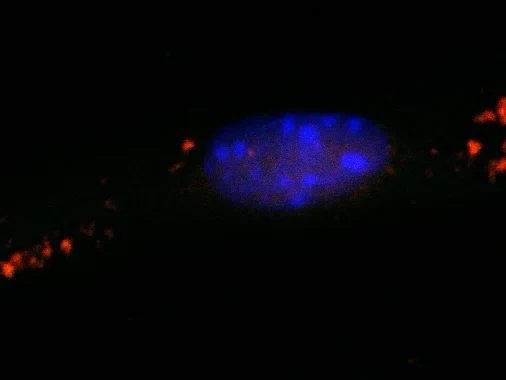
Das sprichwörtliche „Gehirnschmalz“ gibt es wirklich: Abgesehen von Wasser besteht unser Denkorgan hauptsächlich aus Lipiden, vereinfacht gesagt: aus Fett. Die Lipide fungieren zum Beispiel als Isolierschicht um die Nervenfasern und verhindern so Kurzschlüsse. Sie sind aber auch ein Hauptbestandteil der dünnen Membranhäutchen, die die Gehirnzellen umgeben.
Sehr häufige Hirn-Lipide sind die sogenannten Sphingolipide. Eines ihrer Abbauprodukte, das S1P, spielt möglicherweise eine zentrale Rolle bei der Entstehung von Alzheimer und anderen Demenzerkrankungen. „Wir haben Mäuse gezüchtet, die in weiten Teilen ihres Gehirns S1P nicht weiter abbauen können“, erklärt Dr. Gerhild van Echten-Deckert. „Die Tiere zeigten daraufhin eine stark verringerte Lern- und Gedächtnisleistung.“
Van Echten-Deckert forscht als Privatdozentin am LIMES-Institut der Universität Bonn (das Akronym steht für „Life and Medical Sciences“). Sie war bislang eine der wenigen Expertinnen weltweit, die sich für die Rolle von S1P im Gehirn interessieren. Die neue Studie könnte das fundamental ändern. Denn die Forscher der Universität Bonn, des Universitätsklinikums Jena, des Deutschen Zentrums für Neurodegenerative Erkrankungen (DZNE) sowie aus San Francisco und Madrid konnten zeigen, welch weit reichende Konsequenzen der gestörte S1P-Abbau hat.
„Selbstfressen“ hält Gehirn gesund
Normalerweise wird das Lipid in verschiedene Teile zerlegt. Eines der Produkte, die dabei entstehen, wird bei einem weiteren Stoffwechselweg dringend benötigt – der so genannten Autophagie. Dieser Mechanismus (wörtliche Übersetzung: „Selbstfressen“) ermöglicht es Zellen, eigene Bestandteile zu verdauen und zu recyceln. So werden die Zellen beispielsweise defekte Proteine oder Zellorganellen los, die ihre Aufgabe nicht mehr erfüllen.
Die intrazelluläre Müllabfuhr arbeitet in zwei Schritten: Zunächst verpackt sie den Abfall in winzigen „Müllsäcken“. Diese verschmelzen dann mit anderen „Beuteln“, die hoch reaktive Enzyme enthalten. Die Enzyme „schreddern“ den Inhalt der Müllsäcke und entsorgen ihn so.
Das Abbauprodukt von S1P ist an der Verpackung des Abfalls in den intrazellulären Müllsäcken beteiligt. „Ohne Abbau von S1P bilden sich weniger geschlossene Müllbeutel; die Autophagie funktioniert dann nicht mehr störungsfrei“, erklärt der Erstautor der Studie Daniel Mitroi, der gerade seine Promotion am LIMES-Institut abgeschlossen hat. „Im Gehirn unserer Mäuse häuften sich daher schädliche Substanzen an. Dazu zählte etwa das Protein APP, das bei der Entstehung der Alzheimer-Erkrankung eine Schlüsselrolle spielt.“
Autophagie ist nicht nur für die korrekte Funktion des Gehirns wichtig. Wenn die intrazelluläre Müllabfuhr irgendwo im Körper nicht richtig arbeitet, sind schwere Krankheiten die Folge. Der Japaner Yoshinori Ohsumi wurde für seine Arbeiten zu diesem lebenswichtigen Mechanismus im vergangenen Jahr mit dem Medizin-Nobelpreis ausgezeichnet.
Die Ergebnisse der aktuellen Studie rücken einen bislang völlig unbeachteten Entstehungsmechanismus für Demenzerkrankungen in den Blick. „Möglicherweise tragen unsere Arbeiten langfristig dazu bei, dass diese Störungen des Gehirns irgendwann einmal erfolgreich behandelt werden können“, hofft Dr. van Echten-Deckert.
Publikation: Daniel N. Mitroi, Indulekha Karunakaran, Markus Gräler, Julie D. Saba, Dan Ehninger, María Dolores Ledesma und Gerhild van Echten-Deckert: SGPL1 (sphingosine phosphate lyase 1) modulates neuronal autophagy via phosphatidylethanolamine production; Autophagy; DOI: 10.1080/15548627.2017.1291471
Kontakt:
Privatdozentin Dr. Gerhild van Echten-Deckert
LIMES-Institut
Universität Bonn
Tel. 0228/732703
E-Mail: g.echten.deckert@uni-bonn.de