Wenn wir an einer Tube Sonnenmilch riechen, werden in den Sinneszellen der Nase elektrische Pulse erzeugt. Über den Riechkolben im Gehirn gelangen sie in die primäre Riechrinde, die sie dann an verschiedene Hirnzentren verteilt. Im Hippokampus und anderen Regionen wird dann zum Beispiel die Erinnerung an längst vergangene Sommerurlaube am Meer heraufbeschworen.
In den letzten Jahrzehnten haben Hirnforscher eine immer genauere Vorstellung davon bekommen, wie Reize im Gehirn verarbeitet werden und welchen Weg die elektrische Erregung dabei nimmt. An vielen Stellen ist dieses Bild aber noch sehr grob. Abhilfe schaffen könnte die Methode, die die Wissenschaftler der Universität Bonn und der University of California in Los Angeles nun vorgestellt haben.
Nervenzellen leiten elektrische Signale über biologische „Kabel“ - die Axone - an andere Nervenzellen weiter. Jede Nervenzelle ist von einer dünnen Membran umhüllt, die sie von ihrer Umgebung trennt. Im Ruhezustand befinden sich an der Außenseite dieser Membran viele positiv geladene Ionen, deutlich mehr als auf der Innenseite. Zwischen Innen und Außen besteht also eine elektrische Spannung. Neurowissenschaftler sprechen auch von einem Membranpotenzial.
Lichterkette für Nervenzellen
Wenn ein Signal eine bestimmte Stelle des Axons passiert, ändert sich dieses Potenzial dort kurzzeitig. „Und diese Änderung können wir sichtbar machen“, erklärt Prof. Dr. Istvan Mody vom Institut für Experimentelle Epileptologie und Kognitionsforschung (IEECR) des Universitätsklinikums Bonn. Dazu hängen die Forscher den Nervenzellen gewissermaßen eine Lichterkette um. Das Besondere daran: Jedes Lämpchen dieser Kette trägt einen spannungsabhängigen Dimmer. Dadurch wird es dunkler, wenn sich das Membranpotenzial am Ort des Lämpchens ändert.
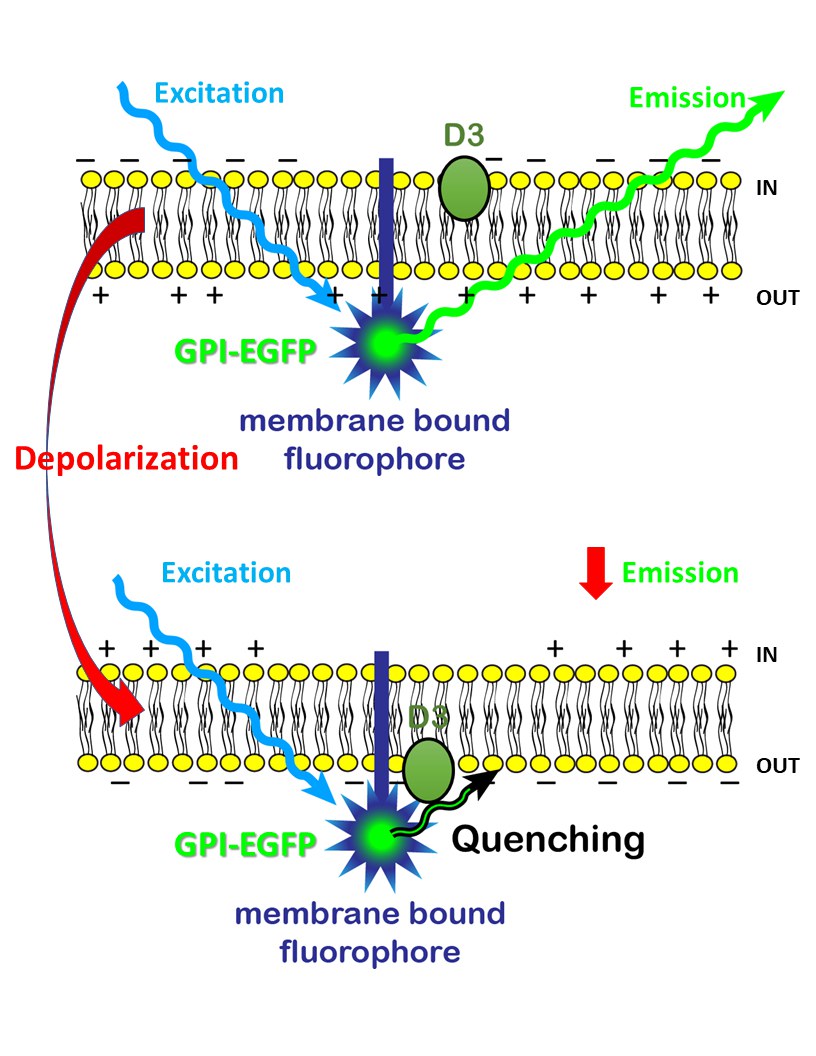
Die Erregungs-Weiterleitung wird auf diese Weise also als eine Art „Dunkelheits-Tropfen“ sichtbar, der am Axon entlangläuft. Als Lichterkette dienen den Forschern dabei fluoreszierende Proteine. „Das Gen dafür haben wir in die Zellen eingeschleust“, erklärt Mody. Die Wissenschaftler haben die Erbanlage zudem mit einer Art Versandetikett versehen. „Dieses Label sorgt dafür, dass die Fluoreszenz-Farbstoffe direkt nach ihrer Herstellung an die Außenseite der Membran transportiert werden. Eine Art Anker stellt dann sicher, dass sie dort bleiben.“
Der Dimmer ist nicht Teil des Nano-Lämpchens, sondern ein weiteres Molekül: ein sogenannter „Dark Quencher“. Normalerweise befindet er sich auf der Innenseite der Membran. Durch die Spannungsänderung bei der Signalweiterleitung wechselt er jedoch nach außen. Dort trifft er auf die Fluoreszenz-Proteine und schirmt sie ab. Das Nano-Lämpchen wird dadurch dunkler. Sobald sich das Potenzial normalisiert, wandert der Dark Quencher zurück auf die Innenseite, und die Leuchtkraft erhöht sich wieder.
„Im Grunde ist diese Methode nicht neu“, sagt Mody. „Wir haben sie aber an zwei Stellen grundlegend verbessert.“ Bislang wurden die Fluoreszenz-Proteine nämlich direkt in die Membran integriert, was die Funktion der Neurone erheblich stört. Die neuen Nano-Lämpchen dagegen sitzen außerhalb der Membran. Sie bleichen zudem nicht so schnell aus, sondern behalten 40 Minuten ihr Leuchtvermögen - viermal so lang wie herkömmliche Fluoreszenz-Farbstoffe.
Hochexplosiver Dimmer
Die zweite Änderung betrifft den Dark Quencher: Die Verbindung, die normalerweise dafür eingesetzt wird, ist giftig und zudem hochexplosiv. Sie wurde sogar im zweiten Weltkrieg als Sprengstoff genutzt. „Unser Quencher ist dagegen völlig ungefährlich“, betont Mody. „Er reagiert außerdem noch schneller und empfindlicher auf kleinste Potenzial-Änderungen. Dadurch lassen sich mit unserer Methode bis zu 100 elektrische Pulse pro Sekunde sichtbar machen.“
Die Methode erlaubt es, die Funktion von Nervenzellen zu beobachten, ohne sie dabei zu stören. Damit wird es zum Beispiel möglich, bei bestimmten neuronalen Erkrankungen einen genaueren Einblick in die damit verbundenen Fehlfunktionen zu bekommen. Letztlich ist sie ein neues vielversprechendes Werkzeug, um die Arbeitsweise des Gehirns besser zu verstehen.
Förderung:
Die Studie wurde durch den European Research Council Advanced Grant 339620 gefördert.
Publikation: Therese C. Alich, Milan Pabst, Leonie Pothmann, Bálint Szalontai, Guido C. Faas, and Istvan Mody: A dark quencher genetically encodable voltage indicator (dqGEVI) exhibits high fidelity and speed. PNAS, https://doi.org/10.1073/pnas.2020235118
Kontakt:
Prof. Dr. Istvan Mody
Institut für Experimentelle Epileptologie und Kognitionsforschung (IEECR)
Universitätsklinikum Bonn
The David Gaffen School of Medicine at UCLA Los Angeles
Tel. +49-228-6885-331
E-Mail: mody@ucla.edu
Therese Christine Alich
Institut für Experimentelle Epileptologie und Kognitionsforschung (IEECR)
Universitätsklinikum Bonn
Tel. +49-228-6885329
E-Mail: ThereseCAlich@uni-bonn.de