Bei einem Infarkt wird der Herzmuskel aufgrund der Mangeldurchblutung irreparabel geschädigt. Gefürchtete Folge sind die so genannten Kammertachykardien und das daraus resultierende Kammerflimmern. Dabei zieht sich der Hohlmuskel unkoordiniert und mit extrem hoher Schlagfolge zusammen. Die Frequenz kann mehr als 300 Schläge pro Minute erreichen. Dieser Zustand ist lebensgefährlich, weil das Blut nicht mehr effektiv durch den Kreislauf gepumpt wird.
Durch die Implantation embryonaler Herzmuskelzellen lässt sich dieses Risiko augenscheinlich drastisch reduzieren - zumindest bei Mäusen. So lautet der Befund von Wissenschaftlern der Universitäten Bonn, Cornell und Pittsburgh in der Zeitschrift Nature. Die Wissenschaftler hatten Mäusen nach einem Infarkt mit diesen Zellen behandelt und dann versucht, durch elektrische Reizung eine Kammertachykardie hervorzurufen. Nur bei gut jedem dritten Tier geriet das Herz ins Stolpern - genauso selten wie bei kerngesunden Nagern. Bei unbehandelten Mäusen nach Herzinfarkt lag diese Quote dagegen praktisch bei 100 Prozent.
Ein paar tausend Zellen reichen
Das abgestorbene Herzgewebe durch neue Muskelzellen zu ersetzen, ist keine ganz neue Idee. Bisher hatten die Ärzte dabei aber vor allem im Blick, die muskuläre Funktion wieder herzustellen. Schließlich gehen bei einem Infarkt viele hundert Millionen Muskelzellen zugrunde. Folge ist oft eine Herzinsuffizienz, die ebenfalls tödlich enden kann. "Diese Herzmuskelschwäche lässt sich mit Ersatzgewebe bis heute nicht beheben", erklärt Professor Bernd K. Fleischmann vom Institut für Physiologie 1. "Zu wenige implantierte Zellen übernehmen wirklich dauerhaft Muskelfunktion. Um Rhythmusstörungen zu verhindern, scheinen dagegen schon ein paar tausend Zellen auszureichen."
Mit den bislang für die Therapie genutzten Skelettmuskelzellen funktioniert das allerdings nicht. "Sie mindern nicht etwa die Gefahr einer Kammertachykardie - im Gegenteil: Die Schwere der Rhythmusstörungen nahm in unserer Studie sogar zu, wenn wir Skelettmuskelzellen verwendeten", betont der Bonner Kardiologe Professor Dr. Thorsten Lewalter.
Grund: Für eine geordnete Kontraktion ist es wichtig, dass die Zellen im Herzmuskel miteinander kommunizieren. Sie geben dazu gewissermaßen das "Schlagsignal" an ihre Nachbarn weiter. "Wirkliche" Herzmuskelzellen verfügen dazu von Natur aus über einen speziellen Kommunikationskanal. Dabei handelt es sich um ein Zelleiweiß namens Connexin 43. "Wir konnten zeigen, dass die von uns implantierten embryonalen Herzmuskelzellen dieses Connexin 43 bilden und darüber das elektrische Signal in die Infarktnarbe einkoppeln", erläutern der Herzchirurg Dr. Wilhelm Röll und der Physiologe Dr. Philipp Sasse.
Neuer Therapieansatz
Wissenschaftlern vom Institut für Genetik ist es gelungen, Skelettmuskel-Zellen derart zu verändern, dass sie ebenfalls Connexin 43 herstellen. Die Forscher testeten auch diese Zellen an Mäusen mit Herzinfarkt - mit Erfolg: Das Risiko einer Kammertachykardie sank auf ein ähnliches Niveau wie bei gesunden Tieren. Diese Entdeckung öffnet möglicherweise die Tür zu einem völlig neuen Therapieansatz. Beim Menschen ist es schließlich aus ethischen Gründen nicht einfach möglich, auf embryonale Herzmuskelzellen zurückzugreifen. "Man könnte aber Stammzellen aus dem Beinmuskel eines Infarktpatienten nehmen und darin das Gen für Connexin 43 einschleusen", sagt Professor Michael I. Kotlikoff von der Cornell-Universität in Ithaca. "Diese veränderten Zellen ließen sich dann in das geschädigte Herz implantieren." Abstoßungsreaktionen wären dabei nicht zu befürchten - schließlich würde es sich um eigene (wenn auch genetisch aufgerüstete) Zellen handeln. Auch Fleischmann spricht von einem wichtigen Zwischenschritt, warnt aber vor zu großen Hoffnungen: "Unsere Ergebnisse gelten für das Mausherz", stellt er klar. "Ob das beim Menschen ebenfalls so klappt, bleibt abzuwarten."
Dass die Studie so erfolgreich verlief, liegt auch an der Interdisziplinarität des Projekts: Allein in Bonn waren mit der Physiologie 1 am Life & Brain Zentrum, den Abteilungen für Herzchirurgie und Innere Medizin II sowie den Instituten für Genetik und Pharmakologie fünf Arbeitsgruppen beteiligt.
Kontakt:
Professor Dr. Bernd K. Fleischmann
Institut für Physiologie 1, Life&Brain-Zentrum, Universität Bonn
Telefon: 0228/6885-200
E-Mail: bernd.fleischmann@uni-bonn.de
Bilder zu dieser Pressemitteilung:
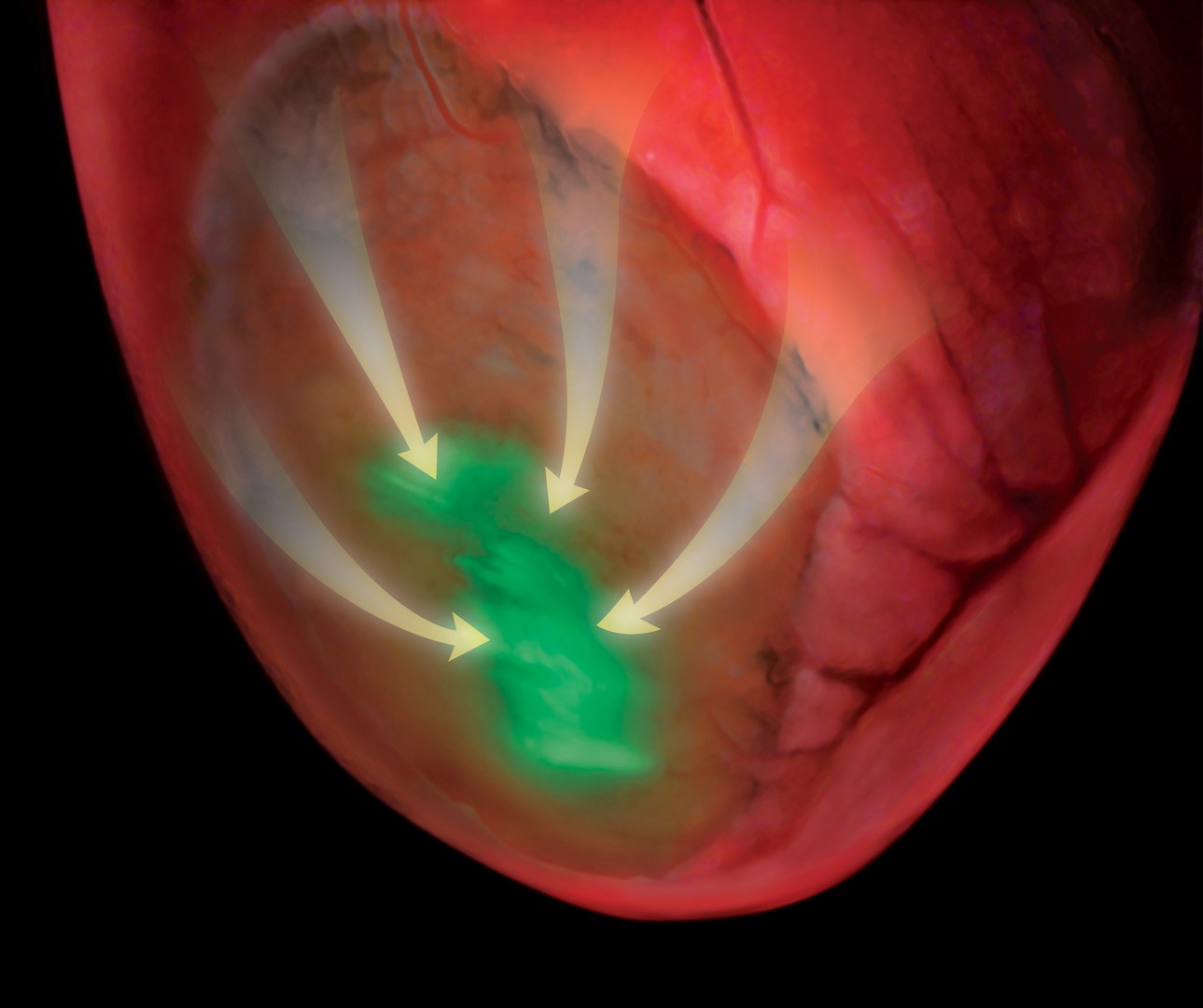
Zum Download einer Bilddatei in Originalauflösung bitte auf die Miniaturansicht klicken. Der Abdruck im Zusammenhang mit der Presseinformation ist kostenlos, dabei ist der angegebene Bildautor zu nennen.Bildzeile:Bonner Forscher berichten zusammen mit US-Kollegen in der neuesten Ausgabe von "Nature", dass die Transplantation von Connexin 43-positiven Muskelzellen in Mäusen das Risiko von Herzrhythmusstörungen nach einem Herzinfarkt reduziert. Dies ist auf eine verbesserte elektrische Kopplung (Pfeile) zurückzuführen. Die transplantierten Zellen (grün) bilden ein Molekül, das bei der Zell-Zellkopplung während des Herzschlags aktiviert wird.Bildautor: Michael Simmons, MFA