Kammerflimmern! Wenn der Herzmuskel rast und sich nicht mehr geordnet zusammenzieht, droht aufgrund fehlender Blutzirkulation der Tod. In so einem Notfall hilft ein Defibrillator, durch starke Stromstöße die normale Herzaktivität wieder herzustellen. Bei Patienten mit bekanntem Risiko für solche Rhythmusstörungen ist die prophylaktische Implantation eines miniaturisierten „Defis“ das Mittel der Wahl. Bei Kammerflimmern wird dann automatisch ein Stromstoß ausgelöst, der die Herzmuskelerregung normalisiert und dadurch das Leben rettet.
„Wenn ein implantierter Defibrillator auslöst, was leider auch durch falsche Detektion der Rhythmusstörung passieren kann, ist das immer ein sehr traumatisches Ereignis für die Patienten“, sagt der Leiter der Studie, Juniorprofessor Dr. med. Philipp Sasse vom Institut für Physiologie I der Universität Bonn. „Der starke elektrische Stromschlag ist sehr schmerzhaft und kann auch das Herz weiter schädigen.“ Deshalb forscht Prof. Sasses Arbeitsgruppe an den Grundlagen für eine schmerzfreie und schonendere Alternative. Wie die Wissenschaftler nun zeigen, lässt sich Kammerflimmern auch durch einen optischen Defibrillator beenden.
Gene für optisch aktivierbare Proteine werden eingeschleust
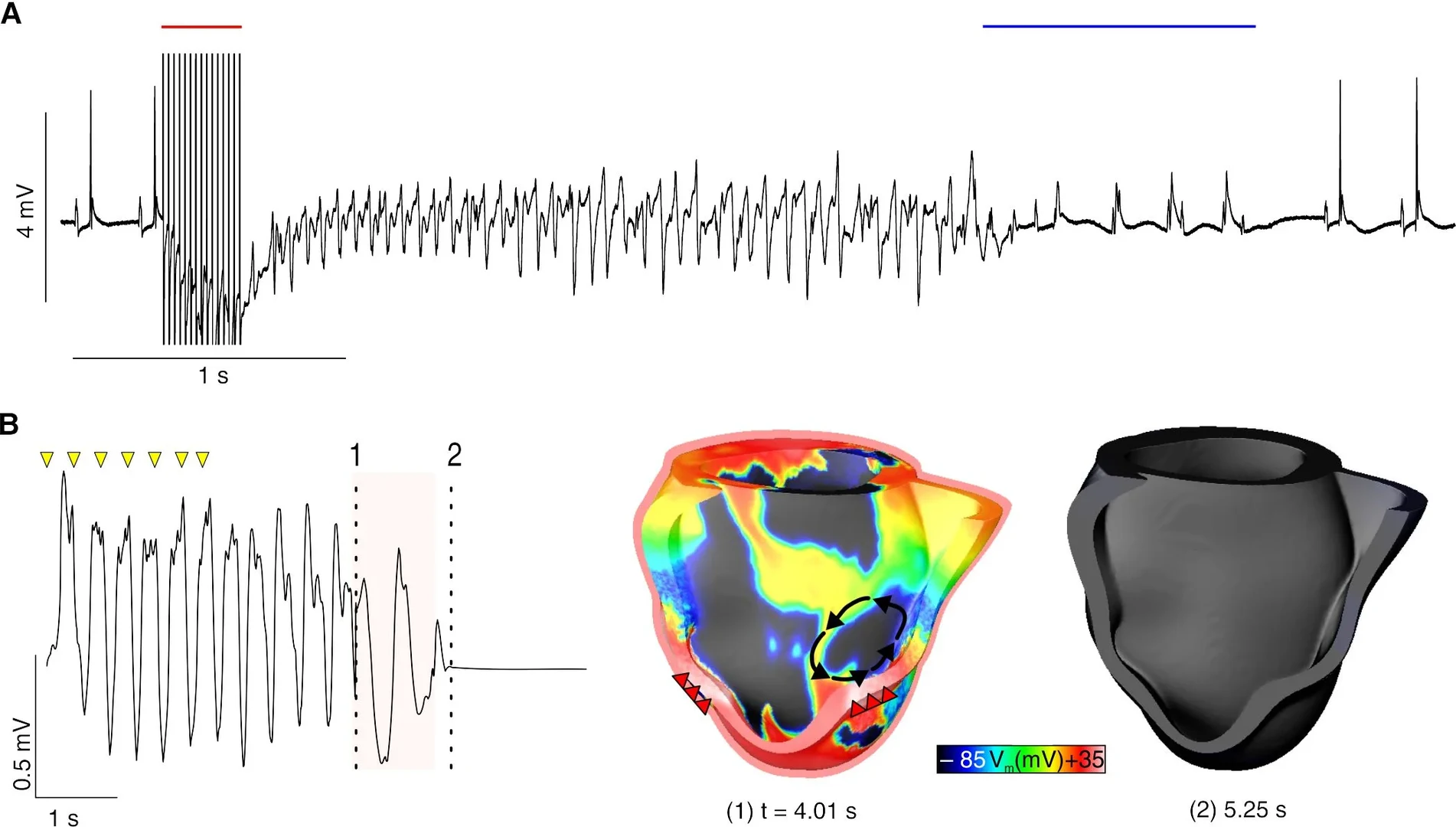
Das Team verwendete die neue Methode der „optogenetischen“ Stimulation und arbeitete dafür mit Mäusen, bei denen die Gene für sogenannte Kanal-Rhodopsine ins Herz eingeschleust wurden. Es handelt sich dabei um Kanäle aus Grünalgen, die unter Einfluss von Licht wie ein Schalter die Durchlässigkeit von Ionen durch die Herzmuskelzellen verändern. Wurde durch die Forscher bei den Mäuseherzen nun ein Kammerflimmern ausgelöst, genügte ein Lichtpuls von einer Sekunde auf das Herz, um den normalen Rhythmus wieder herzustellen. „Das ist ein sehr wichtiges Ergebnis“, betont Erstautor Dr. med. Tobias Brügmann aus Prof. Sasses Team. „Es zeigt erstmals experimentell in Herzen, dass die optogenetische Stimulation zur Defibrillation von Herzrhythmusstörungen genutzt werden kann.“ Das funktionierte auch in ganz normalen Mäusen, welche das Kanal-Rhodopsin erst durch Injektion eines biotechnologisch hergestellten Virus erhielten. Dies zeige eine mögliche klinische Anwendbarkeit, da ähnliche Viren bereits für Gentherapie von Patienten verwendet werden können.
Simulationen zeigen: Erkenntnisse sind auf Menschen übertragbar
Sind aber die an Mäuseherzen gewonnenen Erkenntnisse auch auf Menschen übertragbar? Um diese Frage zu beantworten, arbeiteten die Wissenschaftler der Universität Bonn mit dem „Computational Cardiology” Labor von Prof. Natalia Trayanova am Institut für Computermedizin und biomedizinisches Ingenieurwesen der Johns Hopkins Universität (Baltimore, USA) zusammen. Dort wurde die optogenetische Defibrillation in einem Computermodell von einem Herzen eines Patienten nach Herzinfarkt erprobt. „Unsere Simulationen zeigen, dass ein Lichtpuls auf das Herz auch die Herzrhythmusstörung dieses Patienten beenden würde“, berichtet Prof. Dr. Partrick Boyle, der ebenfalls die Erstautorenschaft innehat. Hierfür musste das Verfahren der Universität Bonn jedoch noch für menschliche Herzen optimiert werden, indem die Herzzellen nicht mit blauem Licht wie bei den Mäusen, sondern mit rotem Licht angeregt wurden. Dieser Aspekt der Studie zeigt die wichtige Rolle von Computermodellen für die systematische Entwicklung optogenetischer Therapieansätze.
Optogenetischer „Defi“ ist prinzipiell machbar
„Unsere Daten zeigen die prinzipielle Machbarkeit eines optogenetischen Defibrillators zur Behandlung von Kammerflimmern“, fasst Prof. Sasse zusammen. Das flimmernde Herz mit einem Lichtreiz wieder in einen normalen Rhythmus zu versetzen, sei absehbar schmerzfrei und deutlich schonender für die Patienten als die Verwendung von Elektroschocks. Das neue Verfahren befinde sich aber noch im Stadium der Grundlagenforschung. Bis ein optischer „Defi“ für die Behandlung von Patienten entwickelt werden könne, dauere es noch mindestens fünf bis zehn Jahre, schätzt Prof. Sasse.
Publikation: Optogenetic defibrillation terminates ventricular arrhythmia in mouse hearts and human simulations, „Journal of Clinical Investigation“, DOI: 10.1172/JCI88950
Kontakt für die Medien:
Juniorprof. Dr. Philipp Sasse
Institut für Physiologie I
Universität Bonn
Tel. 0228/6885212
E-Mail: philipp.sasse@uni-bonn.de
Dr. Tobias Brügmann
Institut für Physiologie I
Universität Bonn
Tel. 0228/6885217
E-Mail: tbruegmann@uni-bonn.de