Flüssiges Wasser besteht zum überwiegenden Teil aus neutralen H2O-Molekülen. Diese können jedoch spontan zerfallen. Dabei entstehen ein negativ geladenes Hydroxid-Ion sowie ein positiv geladenes Hydronium-Ion. Diese Reaktion ist ausgesprochen selten: Auf zehn Milliarden Wassermoleküle kommen nur 36 Ionen.
So verschwindend klein diese Zahl ist: Theoretisch müsste sie noch viel niedriger sein. Die Bindungskräfte innerhalb des Wassermoleküls sind so stark, dass ein spontaner Zerfall extrem unwahrscheinlich ist. Auch tendieren die Ionen dazu, sich direkt wieder zu verbinden. In flüssigem Wasser laufen jedoch Prozesse ab, die seine „Eigendissoziation“ (so das Fachwort für dieses Phänomen) fördern.
„Bei der Quantifizierung dieser Prozesse tappten die Chemiker aber bislang im Dunkeln“, erklärt Dr. Eva Perlt vom Institut für Physikalische und Theoretische Chemie der Universität Bonn. „Dabei bildet die Eigendissoziation die Grundlage für viele Säure-Base-Reaktionen – also für alles, was mit dem pH-Wert zusammen hängt.“ Ohne diese zentrale Eigenschaft wäre Leben, wie wir es kennen, wohl nicht denkbar.
Klassische Simulation am Rechner zu aufwändig
Theoretische Chemiker nutzen heute Computermodelle, um bestimmte Reaktionen besser zu verstehen. Der Zerfall der Wassermoleküle entzieht sich jedoch klassischen Simulationen. „Da die Eigendissoziation so selten ist, müssten wir dazu im Rechner viele Milliarden Teilchen simulieren“, erklärt Perlt. „Das übersteigt schlicht die Leistung der heute verfügbaren Hardware.“
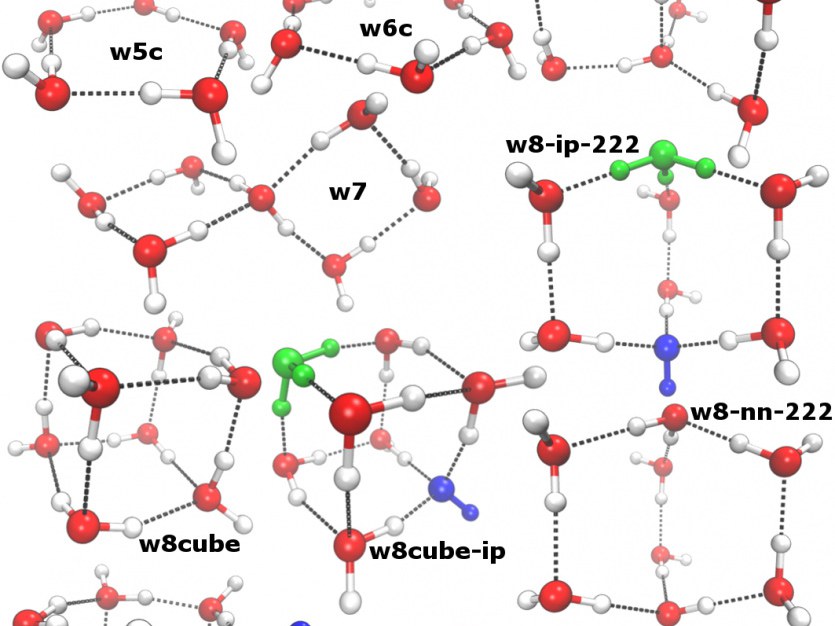
Das internationale Forscherteam hat daher einen anderen Weg beschritten. Wassermoleküle sind polar; sie haben wie kleine Magneten gewissermaßen einen Nord- und einen Südpol. In Lösung ordnen sie sich daher zu lockeren räumlichen Strukturen an, so genannten Clustern. Manche dieser Cluster bieten ein Milieu, in dem sich Ionen besonders wohl fühlen. Sie schaffen also eine Art Mikroumgebung, die die Eigendissoziation fördert.
„Wir haben nun in unserem Modell berechnet, welche Arten von Clustern in flüssigem Wasser vorliegen“, erklärt Prof. Dr. Barbara Kirchner, Leiterin des „Mulliken Center for Theoretical Chemistry“ an der Universität Bonn. „Dadurch konnten wir die Komplexität des Modells erheblich reduzieren. Aus der Zusammensetzung der Cluster konnten wir dann auf die Wahrscheinlichkeit schließen, mit der die Wassermoleküle dissoziieren.“
Das Ergebnis der Berechnung deckt sich hervorragend mit den Werten, die sich in der Natur beobachten lassen. Dem transatlantischen Forscherteam gelang es auch, die Temperaturabhängigkeit des Zerfalls nachzuvollziehen. „Zwischen dem Schmelz- und dem Siedepunkt des Wassers nimmt die Selbstdissoziation um etwa den Faktor 1000 zu“, erläutert Prof. Dr. Ralf Ludwig von der Universität Rostock. „Diese Zunahme wird auch von unserer Computersimulation vorhergesagt.“
Publikation: Eva Perlt, Michael von Domaros, Barbara Kirchner, Ralf Ludwig & Frank Weinhold: Predicting the Ionic Product of Water; Scientific Reports; DOI:10.1038/s41598-017-10156-w
Kontakt:
Prof. Dr. Barbara Kirchner
Institut für Physikalische und Theoretische Chemie
Universität Bonn
Tel. 0228/7360442
E-Mail: kirchner@thch.uni-bonn.de
Dr. Eva Perlt
Institut für Physikalische und Theoretische Chemie
Universität Bonn
Tel. 0228/7360148
E-Mail: eva.perlt@uni-bonn.de